Soal dan Pembahasan Kimia (Saintek) Bagian 2
-
Suatu sel elektrokimia dengan elektrode Zn dan Ag pada keadaan standar menghasilkan arus 0,75 A selama 321 menit. Diketahui nilai
E0 Zn2+ I Zn = - 0,76 V
E0 Ag+ I Ag = + 0,8 V
Maka pengurangan massa di anoda adalah .... gram (F = 96.500 C)
Jawaban : bKatoda : Ag+ + e → Ag
Anoda : Zn → Zn2+ + 2e-
Wanoda =
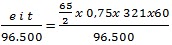 = 4,875 gram
= 4,875 gram -
Proses pemurnian belerang yang dilakukan oleh Frasch dikenal juga dengan proses penambangan sumur panas. Konsep kerjanya adalah dengan mengalirkan air panas kedalam sumur galian yang terdapat deposit belerang, sehingga belerang akan meleleh dan mengapung pada permukaan air. Namun diawal proses ini, Frasch mengalami permasalahan. Suhu tertinggi dari air panas adalah 100oC, namun belerang memiliki titik lebur pada suhu 101,6o C.
Analisis, cara manakah di bawah ini yang paling tepat untuk menyelesaikan masalah yang dihadapai Frasch? (diketahui
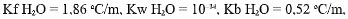 Ar S = 32 g/mol, Ar H = 1 g/mol, O = 16 g/mol).Jawaban : b
Ar S = 32 g/mol, Ar H = 1 g/mol, O = 16 g/mol).Jawaban : b(A) Jawaban A salah, karena menaikan tekanan air akan menggugurkan tanah meningkatkan sedimen, sehingga lebih sulit untuk mendapat belerang murni.
(B) Jawaban B benar. Menambahkan 0,09 kg NaCl atau 90 gram NaCl disetiap liter air akan menaikan suhu air sekitar 1,6oC (sehingga titik didih menjadi air 101,6oC) dan sama dengan titik leleh belerang dalam deposit, sehingga belerang akan didapatkan.
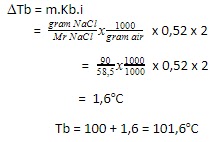
(C) Jawaban C salah. Menambahkan HCl akan merusak alat – alat pertambangan yang umumnya dari logam.
(D) Menambahkan alkohol 10% pada setiap liter air tidak berpengaruh, karena belerang tidak larut dalam alkohol.
(E) Meningkatkan volume air yang masuk tidak akan mempengaruhi, karena konsep kerjanya adalah melelehkan belerang.
-
SEBABJawaban : a

-
Diketahui reaksi redoks (belum setara):
PbSO4(s)+H2O(l)→Pb(s)+PbO2(s)+H2SO4(aq)
Pernyataan berikut ini yang benar adalah ....
- PbSO4 berperan sebagai oksidator
- PbSO4 berperan sebagai reduktor
- Pada akhir reaksi pH laturan lebih kecil dari 7
- Perbandingan mol PbSO4 terhadap H2O adalah 1:2
Jawaban : a
Pernyataan yang benar adalah 1, 2, dan 3.
-
Jawaban : b

-
30
60
120
180
360
Jawaban : b
Sehingga dapat dimasukkan:

-
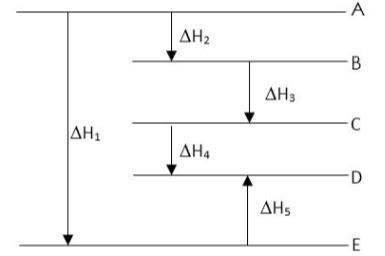
Pernyataan berikut ini yang benar mengenai diagram energi di atas adalah....
Jawaban : c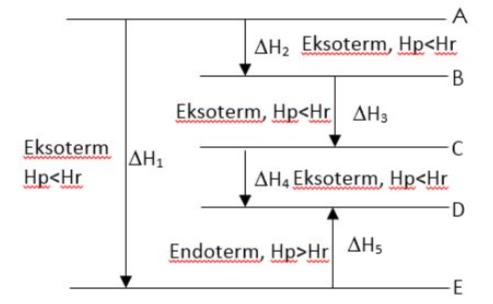
Pada reaksi ekstorem, terjadi perpindahan kalor dari sistem ke lingkungan, sehingga suhu lingkungan akan meningkat. Sebaliknya, pada reaksi endoterm terjadi perpindahan kalor dari lingkungan ke sistem. Sehingga suhu lingkungan akan menurun (menjadi lebih dingin).
-
SEBABJawaban : d
Salah satu faktor yang mempengaruhi kesetimbangan adalah volume. Jika volume diperbesar, maka kesetimbangan akan bergeser ke arah koefisien yang lebih besar. Sebaliknya, jika volume diturunkan maka kesetimbangan akan bergeser ke arah koefisien yang lebih kecil. Pada reaksi H2(g) + I2(g)⇌2HI(g), koefisien kanan dan kiri sama, yaitu 2. Sehingga perubahan volume tidak akan menggeser kesetimbangan atau volume tidak mempengaruhi sistem kesetimbangan ini.
Pernyataan pertama salah dan pernyataan kedua benar.
-
Jawaban : d
Berdasarkan hukum Gay Lussac, untuk reaksi gas maka perbandingan volume = perbandingan koefisien gas – gas yang terlibat dalam reaksi
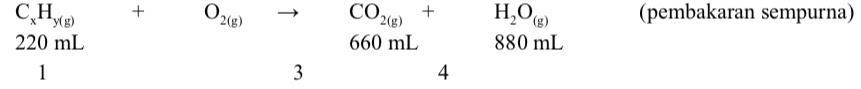
Sehingga,

-
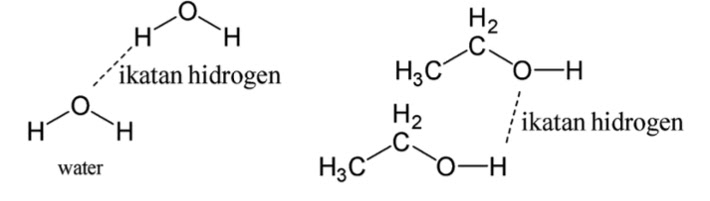
Jawaban : b
Ikatan hidrogen adalah ikatan antarmolekul yang terjadi antara atom atom H dalam satu molekul dengan atom yang lebih elektronegatif yaitu O, N, F pada molekul lain. Karena pada molekul H2O terdapat molekul O dan H, dan pada molekul C2H5OH juga mempunyai ikatan O dan H pada gugus fungsi alkohol sehingga nomor 1 dan 3 akan berinteraksi dengan ikatan hidrogen. Gambaran interaksi antarmolekul H2O dan C2H5OH adalah sebagai berikut: